Модель атомов
Реально рассмотреть строение атома не возможно из-за их малых размеров. По этому строение атома рассматривают с помощью моделей атома. Первая модель атома была создана английским физиком Томсоном, создавшим капельную модель атома. Согласно ей, атом представляет собой шар по объему которого распределён положительный электрический заряд. Внутри шара находятся электроны, количество которых соответствует заряду области.
В 1911 году Резерфорд совместно со своими сотрудниками провел ряд опытов по исследованию состава и строения атома.
 |
 |
 |
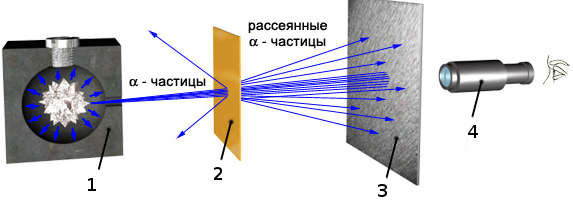
Источник α - лучей помещался в свинцовый контейнер (1). Сначала лучи направлялись непосредственно на экран покрытый слоем кристаллов сульфида цинка способных светиться при попадании на них быстрых заряженных частиц. При наблюдении в микроскоп было обнаружено, что α - частицы мало рассеиваются и попадают в центральную область экрана. (Снимок А). Затем на пути излучения поместили тонкую золотую фольгу (2) и изображение в микроскопе изменилось (Снимок Б). Некоторые α - частицы отклонялись от прямолинейного направления и не попадали в центральную область. Более того, было обнаружено, что часть частиц отражалось от фольги.
Модель атома Томсона не могла объяснить такое поведение α - частиц. Масса частицы во много раз больше массы электрона и для изменения направления ее движения необходимо столкновение с частицей имеющий положительный заряд и массу, соизмеримую с массой иона гелия. Резерфорд предложил иную модель строения атома: внутри атома находится массивное положительно заряженное ядро вокруг которого вращаются электроны. Большая часть массы атома сосредоточено именно в ядре. Из-за сходства модели со строением солнечной системы, модель получила название планетарной.
Домашнее задание: §§ 65, 66









